
L’EFS est au cœur de la médecine de demain. Chaque jour, nos équipes de recherche mettent leur excellence scientifique au service des patients. Lumière sur un programme de recherche innovant pour le traitement d’un cancer de la moelle osseuse.
La découverte de la molécule TLR4 comme facteur clé dans la progression du myélome multiple
Le myélome multiple (MM) est un cancer de la moelle osseuse incurable à ce jour, qui génère de multiples rechutes et effets secondaires. Il se caractérise par une infiltration de cellules cancéreuses (plasmocytes tumoraux) au niveau de la moelle osseuse (MO), substance logée à l’intérieur de l’os et qui permet de fabriquer chaque jour des milliers de cellules souches hématopoïétiques, qui donnent ensuite naissance aux différentes cellules sanguines. Cette pathologie représente 13% des cancers du sang et 5000 nouveaux cas chaque année. Aujourd’hui, les personnes atteintes de ce type de cancer, âgées en moyenne de 65-70 ans, ont une espérance de vie de 5 ans et des symptômes très lourds (douleurs, lésions osseuses, anémie, insuffisance rénale, infections à répétition…)
Nos chercheurs se sont intéressés à ce cancer par le prisme du microenvironnement, autrement dit le « lieu d’habitat » de ces cellules cancéreuses. Ce microenvironnement est constitué de cellules particulières appelées « cellules stromales mésenchymateuses (CSM) ». Ils ont alors constaté que la molécule TLR4, dont le rôle dans notre organisme est de reconnaître les pathogènes, était exprimée en quantité hautement anormale dans les CSM de moelle osseuse chez les patients malades. De manière intéressante, l’expression du TLR4 évoluait en parallèle à l’évolution de la maladie chez les patients (augmentation de l’expression du TLR4 dans les rechutes, diminution de l’expression du TLR4 dans les rémissions).
Le blocage de la molécule TLR4 et son association à d’autres approches thérapeutiques pour freiner la progression de la maladie
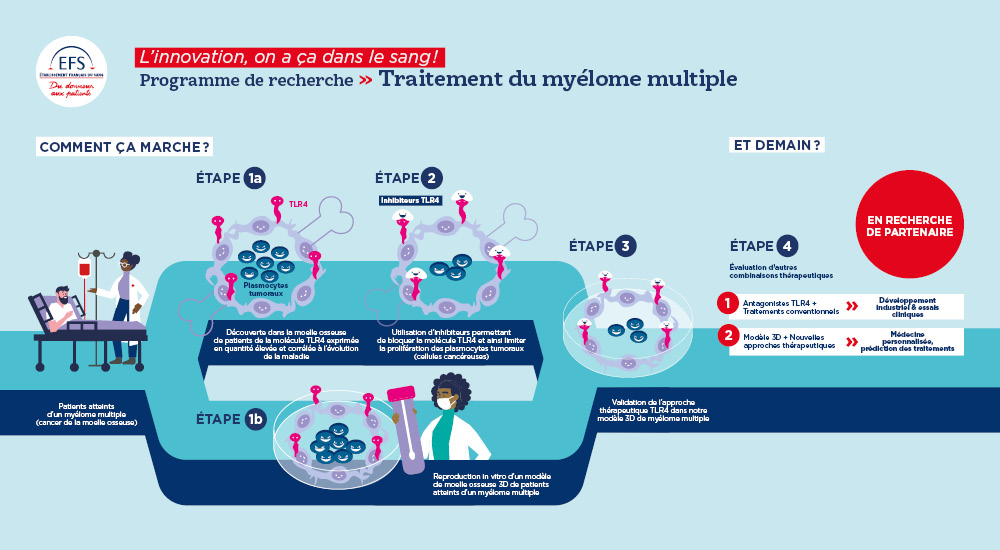
Le projet, en bref ? Dans le MM, nos chercheurs sont les premiers à avoir développé une stratégie thérapeutique qui cible le micro-environnement des cellules cancéreuses, et non uniquement les plasmocytes tumoraux. Ils ont démontré qu’en utilisant des inhibiteurs de la molécule TLR4, qui visent à bloquer son activité, la prolifération des cellules cancéreuses de patients MM était ainsi freinée. Ces expérimentations ont également été confirmées sur un modèle 3D de MO, mis au point par nos équipes, qui permet de reconstituer in vitro la MO d’un patient atteint de ce cancer.
Comment ça marche ?
D’une part le ciblage du microenvironnement par le TLR4 donne un autre angle d’attaque aux traitements anti MM en cours avec des combinaisons synergiques avec les traitements conventionnels tels que chimiothérapies et autres immunosuppresseurs. Cette preuve de concept a été démontrée dans des cocultures de cellules humaines et également à l’échelle d’un organisme entier tel que la souris.
Afin d’aller plus loin dans la précision thérapeutique, les chercheurs ont mis au point, en parallèle, un modèle 3D de MM à base de cellules directement récupérées chez le patient. Ainsi, il est possible de tester les combinaisons susmentionnées dans un contexte plus proche de la pathologie humaine. Cet outil technologique transposable à d’autres pathologies hématologiques s’inscrit dans la médecine personnalisée ayant pour but d’optimiser les traitements cliniques et éviter ainsi les rechutes des patients.
Quels en sont les avantages ?
1) L’approche thérapeutique TLR4
Le fait d’attaquer la maladie sur deux fronts (microenvironnement et cellules cancéreuses) a plusieurs avantages : l’effet thérapeutique est amélioré. Cette approche pourrait permettre de baisser les coûts et les doses de traitements conventionnels et potentiellement diminuer les effets secondaires, souvent très lourds, chez les patients.
2) La modélisation de la maladie in vitro
Le fait d’utiliser des cellules primaires de patients (CSM pour le microenvironnement et plasmocytes tumoraux) nous a permis de générer un modèle in vitro de MM humain en 3D, en nous basant sur la technologie des organoïdes. Ce modèle dans le sillage de la médecine personnalisée permet de tester différentes combinaisons thérapeutiques, afin d’adapter au mieux le traitement en fonction des caractéristiques de chaque patient. Les grands avantages de ce modèle pré-clinique résident dans sa rapidité de mise en œuvre, son coût et sa proximité avec la physiopathologie humaine lui permettant d’être prédictif.
Quelles sont les prochaines étapes ? Protégée par une famille de brevets depuis 2016, cette nouvelle approche thérapeutique ciblant le microenvironnement a récemment fait l’objet d’une publication dans la revue scientifique « Blood Advances », valorisant ainsi le travail initié il y 10 ans et consolidant la demande de brevet afin de faciliter le transfert de technologie vers l’industrie. Il s’agit désormais de trouver un partenaire industriel afin de développer cette stratégie thérapeutique prometteuse et initier la phase d’essais cliniques qui permettra, à terme, d’intégrer cette approche au parcours de soin des patients.
Vous êtes intéressé par un partenariat ? Contactez la direction de la recherche et de la valorisation de l’EFS.
En savoir plus sur l’équipe de recherche
Ce projet a été initié et mené par le Dr Nicolas Espagnolle et ses proches collaborateurs EFS, dont le technicien Jean-Gérard Descamps et l’ingénieure Mélanie Gadelorge, au sein de l’Unité Mixte de Recherche (UMR) Restore de Toulouse, et avec l’appui des hématologistes (J. Corre, PU-PH) de l’Institut universitaire du cancer de Toulouse (IUC-T).
